1. 단원의 목표
2. 단원의 개관
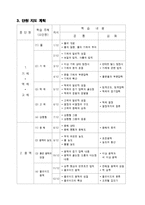
3. 단원 지도 계획
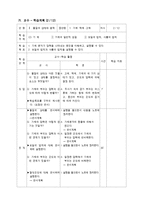
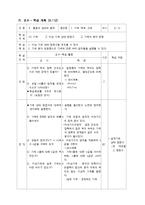
4. 교수 - 학습 자료
3. 전기 분해
전기 분해 반응
(1) 전기 분해의 원리
- 전해질의 수용액이나 용융염에 전극을 담그고 직류 전류를 통하면 그 전해질은 두 전극 에서 화학변화를 일으킨다. 이 변화를 전기 분해(electrolysis) 또는 전해라 한다. 즉, 전 해질은 수용액이나 용융 상태에서 (+), (-)이온으로 전리되고, 전리되어 있는 용액 중 에 직류 전류를 통하면 두 이온은 각각 반대 극으로 끌려가서 전하를 잃고 중성 물질로 된다. 이를 전해라 한다.
① 전기 분해의 원리
전해질 ⇌ (+)이온 + (-)이온
(+)극 : (-)이온 ― e → 중성 단체 (산화)
(-)극 : (+)이온 + e → 중성 단체 (환원)
② 이온화 경향이 큰 이온이나 몇 가지 원자단은 방전하기 어려워 대신 수용액 중의 수소 이온(H+)이나 수산화 이온(OH-) 이 방전하여 H2 기체나 O2 기체가 발생한다.
• 방전하기 어려운 양이온 : K+, Ba2+, Ca2+, Na+, Mg2+ 등
• 방전하기 어려운 음이온 : NO3-, OH-, F-, SO42-, CO32-, PO43- 등

- 오늘 본 자료가 없습니다.
- 인지치료의 이론에 대해서 구체적으로 기술하고 각각의 이론들에 자신의 경우를 대입하여 기술해 보시오
- 한국사회복지사 윤리강령의 주요 내용과 기능에 대해 설명하고, 개정내용에 대해 논하시오
- 한국 사회복지 실천의 과제 및 방향에 대해 설명하고, 본인이 중요하다고 생각하는 한국 사회복지 실천의 발전 방향에 대해 작성하시오
- 카카오톡을 업무용(비즈니스용) 협업도구로 사용하는데 찬성하는지, 찬성한다면 이유는 무엇이고 어떤 이점이 있는지, 반대한다면 어떤 이유인지 기술하시오
- 최근 개인정보보호와 인권이 강화되고 있습니다 감염병관리에서 개인정보보호와 정보공개를 통해 방역관리를 하는 부분이 논의가 되었는데 정보공개를 찬성하는지, 반대하는지를 선택하고, 사회복지자로서 이에 대한 자신의 의견과 이유를 작성하세요
해당 정보 및 게시물의 저작권과 기타 법적 책임은 자료 등록자에게 있습니다. 위 정보 및 게시물 내용의 불법적 이용,무단 전재·배포는 금지되어 있습니다. 저작권침해, 명예훼손 등 분쟁요소 발견 시 고객센터에 신고해 주시기 바랍니다.


















 분야
분야

